Зміст
Назви
Назва: Приглухуватість.
Опис
Приглухуватість. Стійке ослаблення слуху, при якому порушується сприйняття звуків навколишнього світу і мовна комунікація. Ступінь приглухуватості може варіюватися від незначного зниження слуху аж до повної глухоти. Діагностика приглухуватості проводиться отоларингологом і отоневрологом з допомогою комплексу досліджень (отоскопії, аудіометрії, камертональных проб, реєстрації слухових ВП і амоакустичної емісії, імпедансометрії, обертальної проби, стабилографии і тд ). В залежності від форми приглухуватості можуть застосовуватися консервативні (слухопротезування, фізіотерапія, медикаментозна терапія) і хірургічні (тимпанопластика, мірінгопластіка, кохлеарна імплантація і тд ) методи.
Додаткові факти
Приглухуватість – зниження слуху, при якому може мовне спілкування. Глухота – ступінь зниження слуху, при якій хворий не чує слова, вимовлені голосно біля його вуха. Проблема глухоти і приглухуватості набуває великого значення у зв’язку з її широкою поширеністю. В даний час глухота і клінічно значуща приглухуватість спостерігається у 13 млн. Росіян, причому більше мільйона хворих – діти віком до 18 років. Один новонароджений з тисячі народжується з тотальною глухотою чи глибокої приглухуватістю. Порушення слуху виявляються у 14% росіян у віці 45-64 роки та у 30% жителів нашої країни у віці старше 65 років.
Якщо зниження слуху спостерігається з народження або виникло до того, як дитина починає говорити, така приглухуватість називається ранньою. Всі інші випадки порушення слуху відносяться до пізньої приглухуватості. Рання глухота і приглухуватість важче піддаються лікуванню, оскільки пацієнт не знає, що таке звуки і розмовна мова.
Класифікація
Існують класифікації приглухуватості, що враховують рівень ураження, ступінь порушення слуху і період часу, протягом якого розвиваються слухові порушення.
Види приглухуватості в залежності від рівня ураження:
• Кондуктивна приглухуватість.
Викликається перешкодою на шляху проведення і посилення звуку. Перешкода виникає на рівні зовнішнього вуха (вади розвитку, сірчані пробки, пухлини, зовнішній отит) або середнього вуха (травматичне пошкодження барабанної перетинки і слухових кісточок, середній отит, адгезивний отит, тубоотит, отосклероз).
• Нейросенсорна (сенсоневральна) приглухуватість.
На рівні внутрішнього вуха механічні коливання перетворюються в електричні імпульси. Загибель волоскових клітин стає причиною порушення цього процесу. В результаті сприйняття звуків погіршується і спотворюється. При нейросенсорної приглухуватості часто спостерігається зниження больового порогу звукосприйняття. Для здорової людини больовий поріг при сприйнятті звуків становить приблизно 100 дБ. Пацієнти з нейросенсорної приглухуватістю можуть відчувати біль при сприйнятті звуків, незначно перевищують поріг чутності.
Нейросенсорна приглухуватість може розвинутися при мікроциркуляторних порушень у внутрішньому вусі, хвороби Меньєра (підвищення тиску рідини у внутрішньому вусі), патології слухового нерва Причиною нейросенсорної глухоти можуть стати деякі інфекційні захворювання (кір, менінгіт, епідемічний паротит, СНІД). Вкрай рідко до розвитку нейросенсорної приглухуватості призводять аутоімунні захворювання (гранулематоз Вегенера).
Більш чим у 60% пацієнтів з вродженою глухотою і приглухуватістю порушення слуху розвиваються внаслідок токсичного впливу алкоголю на плід при фетальному алкогольному синдромі. При внутрішньоутробному зараженні сифілісом глухим стає кожна третя дитина.
Нейросенсорную приглухуватість можуть викликати лікарські препарати. Необоротне порушення слуху виникає у ряду хворих після прийому антибіотиків аміноглікозидного ряду (мономіцин, канаміцин, неоміцин, гентаміцин). Оборотна приглухуватість може розвиватися при прийомі деяких сечогінних препаратів, антибіотиків з групи макролідів та нестероїдних протизапальних лікарських засобів. Причиною розвитку нейросенсорної глухоти може бути вплив транспортного, побутового та промислового шуму, інтоксикація організму свинцем, ртуттю і окисом вуглецю.
• Змішана приглухуватість.
Розвивається при одночасному впливі факторів, що викликають кондуктивний та нейросенсорную приглухуватість. Для корекції цього виду приглухуватості нерідко потрібні складні слухові апарати.
Види приглухуватості в залежності від періоду розвитку слухових порушень:
• Раптова глухота.
Порушення слуху розвивається протягом кількох годин. Причиною втрати слуху при раптовій глухоті (раптової приглухуватості) є вплив ряду вірусів (віруси герпесу, свинки і кору), порушення кровообігу в лабіринті, ототоксичну вплив деяких ліків, пухлини і травми.
Через характерної симптоматики та особливостей перебігу раптову глухоту (раптову нейросенсорную приглухуватість) виділяють як самостійну нозологічну одиницю. Пацієнти з раптовою глухотою описують настало порушення слуху, як «вимикання» або «обрив телефонного дроту». Ця форма приглухуватості зазвичай буває односторонньою.
Для раптової приглухуватості характерна висока ступінь погіршення слуху, аж до повної глухоти з перших годин захворювання. Приблизно у половини пацієнтів через кілька днів після появи симптомів раптової глухоти настає самовилікування. У деяких хворих порушення слуху носить незворотний характер. Можливо як повне, так і часткове відновлення слуху.
• Гостра приглухуватість.
Порушення слуху розвивається протягом декількох діб. У випадку, коли розвиток приглухуватості триває більше семи днів, але не менше одного місяця, прийнято говорити про підгострій приглухуватості.
• Хронічна приглухуватість.
Слух пацієнта знижується поступово, протягом місяців або навіть років. Виділяють стабільну та прогресуючу стадію хронічної приглухуватості.
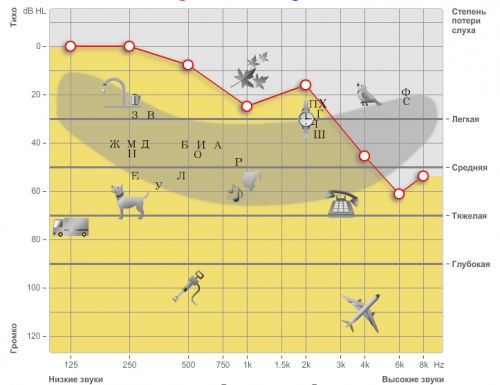
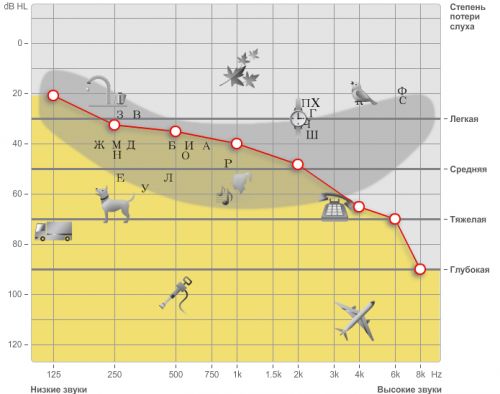
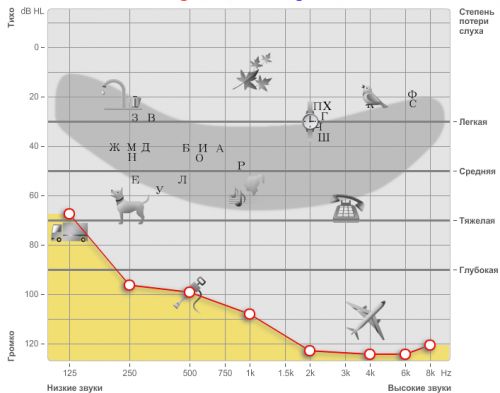
При всіх видах приглухуватості можуть спостерігатися різні ступені зниження слуху – від легкої приглухуватості до повної глухоти. Ступеня приглухуватості:
• I ступінь – втрата слуху, при якій пацієнт не сприймає звуки мовного діапазону, що не перевищують 26-40 дБ;
• II ступінь – втрата слуху, при якій пацієнт не сприймає звуки мовного діапазону, що не перевищують 41-55 дБ;
• III ступінь – втрата слуху, при якій пацієнт не сприймає звуки мовного діапазону, що не перевищують 56-70 дБ;
• IV ступінь – втрата слуху, при якій пацієнт не сприймає звуки мовного діапазону, що не перевищують 71-90 дБ.
У випадку, коли хворий не чує звуки мовного діапазону потужністю понад 90 дБ, йому виставляється діагноз «глухота».
Діагностика
У процесі діагностики глухоти і приглухуватості важливо виявити не тільки ступінь порушення слуху. Необхідно максимально точно визначити причину порушення слуху, рівень ураження, стійкість приглухуватості, її прогресування або регрессирование. Попереднє розпізнавання глухоти і вираженою приглухуватості не представляє труднощів і проводиться отоларингологом. Застосовується мовна аудіометрія (розмовна і шепотная мова). При виявленні приглухуватості необхідна консультація сурдолога. Для розпізнавання приглухуватості легкого ступеня використовується спеціальна апаратура (аудіометри, камертони ).
Диференціальна діагностика
Диференціювання між кондуктивної приглухуватістю (ураженням звукопровідного апарату) та нейросенсорної приглухуватістю (патологією апарату звукосприйняття) проводиться за допомогою аудіометрії та отоскопії. У пацієнтів з кондуктивної приглухуватістю при отоскопії можуть виявлятися перфоративні або рубцеві зміни барабанної перетинки. У ряді випадків (рубці на барабанній порожнині, зрощення стремечка, молоточка і ковадла) зміни при проведенні отоскопического дослідження не виявляються. Рухливість звукопровідною системи оцінюється за допомогою пневматичної воронки Зигле.
Істотну допомогу в процесі диференціальної діагностики між кондуктивної і нейросенсорної приглухуватістю надає порівняльна оцінка повітряної і кісткової провідності. При кондуктивної приглухуватості повітряна звукопровідність погіршується, а кісткова зберігається на нормальному рівні або навіть поліпшується. Для нейросенсорної приглухуватості характерно погіршення як повітряного, так і кісткової провідності. На аудіограмі пацієнта з кондуктивної приглухуватістю виявляється значний розрив між лініями кісткової та повітряної провідності, на аудіограмі хворого з нейросенсорної приглухуватістю лінії провідності зливаються.
Для визначення локалізації рівня ураження слухового нерва і диференціальної діагностики між нейросенсорної і корковою (що з’явилася в результаті пошкодження відповідних ділянок головного мозку) глухотою необхідна консультація отоневролога. Застосовуються спеціальні обстеження (порогова аудіометрія, тонова аудіограма, дослідження слухових ВП ).
Значні труднощі виникають при виявленні приглухуватості і глухоти у дітей раннього віку. Для оцінки стану слуху в цьому випадку застосовується комп’ютерна аудіометрія і акустична імпедансометрія середнього вуха.
Лікування
• Лікування кондуктивної приглухуватості.
При порушенні функціональності або цілісності слухових кісточок і барабанної перетинки зазвичай потрібне оперативне лікування. Існує велика кількість хірургічних операцій, які забезпечують повне відновлення або істотне поліпшення слуху (протезування слухових кісточок, тимпанопластика, мірінгопластіка ). У ряді випадків відновлення слуху можливо навіть при повній глухоті. Вид оперативного втручання визначається характером поразки звукопровідною системи.
• Лікування нейросенсорної приглухуватості.
Загибель волоскових клітин незворотна незалежно від причини їх поразки. Коригувати порушення хірургічним шляхом неможливо. На початкових стадіях захворювання при точній постановці діагнозу у ряді випадків хороший ефект дає лікарська терапія в поєднанні з физиолечением, електростимуляцією і оксигенобаротерапией. Єдиним способом компенсації при значній давності захворювання, глухоту і важкої двосторонньої нейросенсорної приглухуватості було і залишається слухопротезування. Підбір установка і настроювання слухового апарату здійснюється лікарем-слухопротезистом.
Завдяки сучасним досягненням медицини розроблено оперативні методи лікування нейросенсорної приглухуватості і альтернативою слухового апарату стала кохлеарна імплантація.
Профілактика
Основним профілактичним заходом щодо попередження глухоти і приглухуватості є масове обстеження. Регулярні обстеження показані всім працівникам шумних виробництв та іншим категоріям населення, які входять до групи підвищеного ризику. Дуже важливо своєчасно виявляти ознаки туговухості у дітей, оскільки не виявлені вчасно порушення слуху можуть стати причиною затримки формування мови і відставання в інтелектуальному розвитку.
Основні медпослуги за стандартами лікування
|
||||||||||||||
Клініки для лікування з найкращими цінами
|
||||||||||||||
| НИАРМЕДИК на Маросейка | 7(499) 969..показатиЗапис: 7(499) 116-82-39
7(499) 969-21-29 7(495) 617-11-71 |
Москва (м. Китай-Місто) | 14780ք(80%*) | |||||||||||
| НИАРМЕДИК на Гамалії | 7(499) 969..показатиЗапис: 7(499) 116-82-39
7(499) 969-24-57 7(495) 617-11-71 |
Москва (м. Щукінська) | 14780ք(80%*) | |||||||||||
| НИАРМЕДИК на проспекті Маршала Жукова | 7(499) 519..показатиЗапис: 7(499) 116-82-39
7(499) 519-37-10 7(495) 617-11-71 |
Москва (м. Хорошево) |
— |
14780ք(80%*) | ||||||||||
| Будь Здоровий в Останньому провулку | 7(495) 782..показатиЗапис: 7(499) 116-82-39
7(495) 782-88-82 7(495) 663-03-03 |
Москва (м. Сухаревская) | 16845ք(80%*) | |||||||||||
| Будь Здоров на Ліговському | 7(812) 448..показатиЗапис: 7(499) 116-82-39
7(812) 448-88-82 |
Санкт-Петербург (м. Московські ворота) | 8440ք(70%*) | |||||||||||
| НИАРМЕДИК на Псковській | 7(499) 116..показати 7(499) 116-77-32
7(495) 617-11-71 |
Москва (м. Алтуфьево) | — | 14780ք(70%*) | ||||||||||
| НИАРМЕДИК на Барклая | 7(495) 617..показати 7(495) 617-11-71 | Москва (м. Багратионовская) | — | 14780ք(70%*) | ||||||||||
| НИАРМЕДИК у 2-му проїзді Боткинском | 7(499) 116..показати 7(499) 116-77-38
7(495) 940-67-06 7(495) 778-50-59 |
Москва (м. Динамо) | — | 14780ք(70%*) | ||||||||||
| НИАРМЕДИК на Варшавському шосе | 7(495) 617..показати 7(495) 617-11-71 | Москва (м. Нагатинська) | — | 14780ք(70%*) | ||||||||||
| * – клініка надає 100% з обраних послуг. Детальніше при натисканні на ціну. | ||||||||||||||
Назви
Російська назва: Триметазидин.
Англійська назва: Trimetazidine.
Латинська назва
Trimethazidinum ( Trimethazidini).
Хімічна назва
1-[(2,3,4-Триметоксифенил)метил]піперазин (у вигляді дигідрохлориду).
Фарм Група
• Антигіпоксантів і антиоксиданти.
Нозології
• H31,1 Дегенерація судинної оболонки ока.
• H34 Оклюзії судин сітківки.
• H81,0 Хвороба Меньєра.
• H81,4 Запаморочення центрального походження.
• I20 Стенокардія [грудна жаба].
• I25 Хронічна ішемічна хвороба серця.
• I42 Кардіоміопатія.
• R07,2 Біль в області серця.
Код CAS
5011-34-7.
Фармакодинаміка
Фармакологічна дія – антигіпоксичну, що регулює енергетичний метаболізм.
Фармакодинаміка.
Механізм дії. Триметазидин запобігає зниження внутрішньоклітинної концентрації АТФ шляхом збереження енергетичного метаболізму клітин у стані гіпоксії. Таким чином триметазидин забезпечує нормальне функціонування мембранних іонних каналів, трансмембранний перенос іонів калію і натрію та збереження клітинного гомеостазу.
Триметазидин інгібує окислення жирних кислот за рахунок селективного інгібування ферменту 3-кетоацил-КоА-тіолази — мітохондріальної длинноцепочечной ізоформи жирних кислот, що призводить до посилення окислення глюкози та прискоренню гліколізу з окисленням глюкози, що і обумовлює захист міокарда від ішемії. Переключення енергетичного обміну з окислення жирних кислот на окислення глюкози лежить в основі фармакологічних властивостей триметазидину.
Фармакодинамічні властивості. Триметазидин підтримує енергетичний метаболізм серця та нейросенсорных тканин під час ішемії; зменшує вираженість внутрішньоклітинного ацидозу і змін трансмембранного іонного потоку, що виникають при ішемії; знижує рівень міграції та інфільтрації полинуклеарных нейтрофілів в ішемізованих і реперфузированных тканинах серця; зменшує розмір пошкодження міокарда; не надає пряме вплив на показники гемодинаміки.
У пацієнтів зі стенокардією триметазидин збільшує коронарний резерв, тим самим сповільнюючи наступ ішемії, спричиненої фізичним навантаженням, починаючи з 15-го дня терапії; обмежує коливання артеріального тиску, викликані фізичним навантаженням, без значних змін ЧСС; значно знижує частоту приступів стенокардії і потреби в прийомі нітрогліцерину короткої дії; покращує скоротливу функцію лівого шлуночка у пацієнтів з ішемічною дисфункцією.
Результати проведених клінічних досліджень підтвердили ефективність і безпека застосування триметазидину у пацієнтів зі стабільною стенокардією, як у монотерапії, так і у складі комбінованої терапії при недостатньому ефекті інших антиангінальних ЛЗ.
У дослідженні з участю 426 пацієнтів зі стабільною стенокардією додавання триметазидину (60 мг/добу) до терапії метопрололом у дозі 100 мг/добу (50 мг 2 рази на добу) протягом 12 тижнів статистично достовірно покращило результати навантажувальних тестів та клінічні симптоми порівняно з плацебо. Загальна тривалість навантажувальних тестів склала 20,1 с (р=0,023), загальний час виконання навантаження 0,54 METs (р=0,001), час до розвитку депресії сегмента ST на 1 мм 33,4 с (р=0,003), час до розвитку нападу стенокардії 33,9 з (р.
У дослідженні з участю 223 пацієнтів зі стабільною стенокардією додавання триметазидину в дозі 35 мг (2 рази на добу) до терапії атенололом у дозі 50 мг (1 раз на добу) протягом 8 тижнів через 12 год після прийому призводило до збільшення часу до розвитку ішемічної депресії сегмента ST на 1 мм ( 34,4 с, р=0,03) при проведенні навантажувальних тестів у підгрупі пацієнтів (N=173) порівняно з групою плацебо. Аналогічні результати отримано і для часу розвитку нападів стенокардії (р=0,049). Не виявлено достовірні відмінності між групами для інших вторинних кінцевих точок (загальна тривалість навантажувальних тестів, загальний час навантаження і клінічні кінцеві точки).
У дослідженні з участю 1962 пацієнтів зі стабільною стенокардію триметазидин в двох дозах (70 і 140 мг/добу) у порівнянні з плацебо був доданий до терапії атенололом 50 мг/добу. В загальній популяції, включаючи пацієнтів без симптомів, так і з симптомами стенокардії, триметазидин не продемонстрував переваг ергометричними (загальна тривалість навантажувальних тестів, час до настання ішемічної депресії сегмента ST на 1 мм і час до розвитку нападу стенокардії) і клінічним кінцевим точкам. Однак у ретроспективному аналізі в підгрупі пацієнтів з симптомами стенокардії (N=1574) триметазидин (140 мг) значно поліпшив загальний час навантажувального тесту ( 23,8 с у порівнянні з 13,1 з плацебо; р=0,001) і час до розвитку нападу стенокардії ( 46,3 з порівняно з 32,5 з плацебо; р=0,005).
Фармакокінетика
Абсорбція.
Пролонговане вивільнення. Після прийому всередину триметазидин має лінійний фармакокінетичний профіль і досягає Cmax в плазмі приблизно через 14 год після прийому. В інтервалах між прийомами ( тд; протягом 24 год) концентрація триметазидину у плазмі крові протягом 15 год після прийому зберігається на рівні не менше 75% від Cmax.
Рівноважний стан досягається після прийому 3-ї дози (через 3 доби). Прийом їжі не впливає на біодоступність триметазидину.
Модифіковане вивільнення. Після прийому всередину триметазидин швидко абсорбується, Tmax в плазмі крові становить приблизно 5.
Понад 24 год концентрація триметазидину у плазмі крові залишається на рівні, що перевищує 75% концентрації, яка визначається через 11 Рівноважний стан достигаетчся через 60 Прийом їжі не впливає на біодоступність триметазидину.
Розподіл. Vd складає 4,8 л/кг, що свідчить про хорошому розподілі триметазидину в тканинах (ступінь зв’язування з білками плазми крові достатньо низька, приблизно 16% in vitro).
Виведення. Триметазидин виводиться в основному нирками, головним чином у незміненому вигляді. T1/2 у молодих здорових добровольців близько 7 год, у пацієнтів старше 65 років — близько 12.
Нирковий кліренс триметазидину прямо корелює з кліренсом креатиніну, печінковий кліренс знижується з віком пацієнта.
Особливі групи пацієнтів.
Пацієнти старше 75 років. У пацієнтів старше 75 років може спостерігатися підвищена експозиція триметазидину з-за вікового зниження функції нирок. Було проведено спеціальне дослідження в популяції пацієнтів старше 75 років при прийомі триметазидину в дозі 35 мг 2 рази на добу. Аналіз, проведений кінетичним популяционным методом, показав в середньому дворазове підвищення експозиції триметазидину у плазмі крові у пацієнтів з тяжким ступенем ниркової недостатності (Cl креатиніну Cl креатиніну 60 мл/хв.
Ніяких особливостей, що відносяться до безпеки триметазидину у пацієнтів старше 75 років порівняно з загальною популяцією, виявлено не було.
Ниркова недостатність. Експозиція триметазидину в середньому була збільшена в 2,4 рази у пацієнтів з нирковою недостатністю помірного ступеня тяжкості (Cl креатиніну 30-60 мл/хв) і в середньому в 4 рази — у пацієнтів з тяжким ступенем ниркової недостатності (Cl креатиніну.
Ніяких особливостей, що відносяться до безпеки триметазидину у цій популяції пацієнтів у порівнянні з загальною популяцією, виявлено не було.
Діти і підлітки. Фармакокінетика триметазидину у дітей та підлітків віком до 18 років не вивчалася.
Показання до застосування
ІХС, стенокардія, ішемічна кардіоміопатія (у складі комплексної терапії), хоріоретинальні судинні порушення, шум у вухах, запаморочення (судинні порушення, хвороба Меньєра).
Тривала терапія ІХС — профілактика нападів стабільної стенокардії у складі моно – чи комбінованої терапії; хоріоретинальні порушення з ішемічним компонентом; вестибулокохлеарные порушень ішемічної природи. Такі як запаморочення. Шум у вухах. Порушення слуху.
Протипоказання
Підвищена чутливість; хвороба Паркінсона, симптоми паркінсонізму, тремор, синдром неспокійних ніг та інші пов’язані з ними рухові порушення; тяжка ниркова недостатність (Cl креатиніну.
Через відсутність достатньої кількості клінічних даних пацієнтам до 18 років призначення триметазидину не рекомендується.
Обмеження до використання
Печінкова недостатність тяжкого ступеня тяжкості (від 10 до 15 балів за шкалою Чайлд-П’ю); ниркова недостатність помірного ступеня тяжкості (Cl креатиніну 30-60 мл/хв); вік старше 75 років ( тд; «Заходи безпеки»).
Застосування при вагітності і годуванні грудьми
Дані про застосування триметазидину у вагітних відсутні. Дослідження на тваринах не виявили наявність прямої або непрямої репродуктивної токсичності. Дослідження репродуктивної токсичності не показали вплив триметазидину на репродуктивну функцію у щурів обох статей. В якості запобіжного заходу не рекомендується застосовувати триметазидин під час вагітності.
Дані про виділення триметазидину або його метаболітів у грудне молоко відсутні. Ризик для немовляти або дитини не може бути виключений. Не слід застосовувати триметазидин в період грудного вигодовування. При необхідності застосування триметазидину в період лактації грудне вигодовування необхідно припинити.
Побічні ефекти
Небажані реакції, визначені як небажані явища, принаймні можливе мають відношення до лікування триметазидином, наведені в наступної градації: дуже часто (≥1/10); часто (≥1/100.
З боку травної системи. Часто – біль у животі, діарея, диспепсія, нудота, блювання; частота невідома – запор.
Загальні розлади. Часто – астенія.
З боку ЦНС. Часто – запаморочення. Головний біль; частота невідома — симптоми паркінсонізму (тремор. Акінезія. Підвищення тонусу). Хиткість ходи. Синдром неспокійних ніг. Інші пов’язані з ними рухові порушення. Зазвичай оборотні після припинення терапії. Порушення сну (безсоння. Сонливість).
З боку шкірних покривів і підшкірно. Жирової клітковини – часто – шкірний висип, свербіж, кропив’янка; частота невідома – гострий генералізований екзантематозний пустульоз, набряк Квінке.
З боку ССС. Рідко – відчуття серцебиття. Екстрасистолія. Тахікардія. Виражене зниження артеріального тиску. Ортостатична гіпотензія. Яка може супроводжуватися загальною слабкістю. Запамороченням або втратою рівноваги. Особливо при одночасному прийомі гіпотензивних препаратів. Припливи крові до шкіри обличчя.
З боку системи кровотворення і лімфатичної системи. Частота невідома – агранулоцитоз, тромбоцитопенія, тромбоцитопенічна пурпура.
З боку печінки та жовчовивідних шляхів. Частота невідома – гепатит.
Взаємодія
Не спостерігалося. Пацієнт повинен повідомити лікаря про всіх прийнятих ЛЗ.
Передозування
Є лише дуже обмежена інформація про передозування триметазидину. У разі передозування слід проводити симптоматичну терапію.
Спосіб застосування та дози
Всередину.
Заходи обережності застосування
Триметазидин не призначений для купірування нападів стенокардії та не показаний для початкового курсу терапії нестабільної стенокардії або інфаркту міокарда на догоспітальному етапі або в перші дні госпіталізації.
У випадку розвитку нападу стенокардії слід переглянути і адаптувати лікування (лікарську терапію або проведення процедури реваскуляризації).
Триметазидин може спричиняти або погіршувати симптоми паркінсонізму (тремор, акінезія, підвищення тонусу), тому слід проводити регулярне спостереження пацієнтів, особливо похилого віку. У сумнівних випадках пацієнти повинні бути направлені до невролога для відповідного обстеження.
При появі рухових порушень, таких як симптоми паркінсонізму, синдром неспокійних ніг, тремор, хиткість ходи, триметазидин слід остаточно скасувати.
Такі випадки рідкісні і симптоми зазвичай проходять у більшості пацієнтів протягом 4 міс після припинення терапії. Якщо симптоми паркінсонізму зберігаються більше 4 міс після відміни, слід проконсультуватися у невролога.
Можуть відзначатися випадки падіння, пов’язані з нестійкістю в позі Ромберга і хиткістю ходи або вираженим зниженням артеріального тиску, особливо у пацієнтів, які приймають гіпотензивні ЛЗ ( тд; «Побічні дії»).
Слід з обережністю призначати триметазидин пацієнтам, у яких можливе підвищення його експозиції, — при помірній нирковій недостатності, у пацієнтів літнього віку старше 75 років.
Вплив на здатність керувати автотранспортом і виконувати роботи, що потребують високої швидкості психомоторних реакцій. У ході клінічних досліджень не було виявлено вплив триметазидину на показники гемодинаміки, однак в період пострегистрационного застосування спостерігалися випадки запаморочення та сонливості ( тд; «Побічні дії»), що може вплинути на здатність керувати автотранспортом і виконувати роботи, що потребують підвищеної швидкості фізичної і психічної реакції.
Опис
Приглухуватість. Стійке ослаблення слуху, при якому порушується сприйняття звуків навколишнього світу і мовна комунікація. Ступінь приглухуватості може варіюватися від незначного зниження слуху аж до повної глухоти.
Діагностика приглухуватості проводиться отоларингологом і отоневрологом з допомогою комплексу досліджень (отоскопії, аудіометрії, камертональных проб, реєстрації слухових ВП і амоакустичної емісії, імпедансометрії, обертальної проби, стабилографии і тд ).
В залежності від форми приглухуватості можуть застосовуватися консервативні (слухопротезування, фізіотерапія, медикаментозна терапія) і хірургічні (тимпанопластика, мірінгопластіка, кохлеарна імплантація і тд ) методи.
Список літератури
GJB2 – «gap junction protein ?2», ген, що кодує білок коннексин 26
ВМП – високотехнологічна медична допомога
ВОАЭ – викликана отоакустическая емісія
Гц – Герц
дБ – децибел
дБ нпр – дб над порогом чутності
ІПРА – індивідуальна програма реабілітації та абилитации
ЗВОАЭ – затримана викликана отоакустическая емісія
КТ – комп’ютерна томографія
ЛП – латентний період
МРТ – магнітно-резонансна томографія
МСЕ – медико-соціальна експертиза
КІ – кохлеарна імплантація
КСВП – коротколатентные слухові викликані потенціали
ОАЕ – отоакустическая емісія
СА – слухові апарати
СВП – слухові викликані потенціали
СНП – сенсоневральна приглухуватість
ЦМВІ – цитомегаловірусна інфекція
ЦНС – центральна нервова система
- Маркова П. Р. Спадкові порушення слуху. В кн.:
Оториноларингологія/ Національне керівництво / під ред. В. Т. Пальчуна
В. Т. 2-е видання. – М.: Геотар, 2016. – 1024 с.
- Morton CC, Nance WE. Newborn hearing screening – a silent revolution. New England Journal of Medicine. 2006; 354: 2151-64.
- Маркова П. Р., Мегрелішвілі С. М., Зайцева Н.Р., Шагіна І. А., Поляків
А. В. ДНК-діагностика при вродженій і ранньої дитячої приглухуватості/глухоті.
Вісник оториноларингології. 2002; 6: 12-15.
- Goderis J, De Leenheer E, Smets K, Van Hoecke H, Keymeulen A, Dhooge
I. Hearing loss and congenital CMV infection: a systematic review.
Pediatrics. 2014; 134: 972-82.
- Andrade GM, Resende LM, Goulart EM, Siqueira AL, Vitor RW, Januario
JN. Hearing loss in congenital toxoplasmosis detected by newborn
screening. Braz J Otorhinolaryngol. 2008; 74: 21-8.
- Westerberg BD, Atashband S, Kozak FK. A systematic review of the
incidence of sensorineural hearing loss in neonates exposed to herpes
simplex virus (HSV). Int J Pediatr Otorhinolaryngol. 2008; 72: 931-7.
- Borg E. Perinatal asphyxia, hypoxia, ischemia and hearing loss. An overview. Scand Audiol. 1997; 26:77-91.
- Akinpelu OV, Waissbluth S, Daniel SJ. Auditory risk of
hyperbilirubinemia term in newborns: a systematic review. Int J Pediatr
Otorhinolaryngol. 2013; 77: 898-905.
- Shapiro SM. Bilirubin toxicity in the developing nervous system. Pediatr Neurol. 2003; 29: 410-21.
- Hille ET, van Straaten HI, Verkerk PH. Prevalence and independent
risk factors for hearing loss in NICU infants. Acta Paediatr. 2007; 96:
1155-8.
- Borkoski-Barreiro SA, Falcon-Gonz?lez JC, Liminana-Canal JM,
Ramos-Macias A. Evaluation of very low birth weight (?1,500 g) as a risk
indicator for sensorineural hearing loss. Acta Otorrinolaringol Esp.
2013; 64: 403-8.
- Cristobal R, Oghalai JS. Hearing loss in children with very low
birth weight: current review of epidemiology and pathophysiology. Arch
Dis Child Fetal Neonatal Ed. 2008; 93: F462–468.
- Рахманова В. В., Дьяконова І. Н., Ишанова Ю. С. Слухова функція
недоношених дітей першого року життя в залежності від термінів гестації
за даними реєстрації амоакустичної емісії. Вісник
оториноларингології. 2011; 6:20-23.
- Савенко В. В., Бобошко М. Ю. Слухова функція у дітей, що народилися недоношеними. Вісник оториноларингології. 2015; 6:71-76.
- Таварткіладзе Р. А., Загорянская М. Е., Румянцева М. Р. та ін Методики
епідеміологічного дослідження порушень слуху// Методичні
рекомендації. – Москва, 2006. – 27 с.
- Fortnum HM, Summerfield AQ, Marshall DH, Davis AC, Bamford
JM. Prevalence of permanent childhood hearing impairment in the United
Kingdom and implications for universal neonatal hearing screening:
questionnaire based ascertainment study.
BMJ. 2001 Sep 8; 323(7312):536-40 - Watkin P, Baldwin M. The
longitudinal follow up of a universal neonatal hearing screen: the
implications for confirming deafness in childhood. International Journal
of Audiology. 2012; 51(7): 519-528.
- Таварткіладзе
Р. А. Функціональні методи дослідження слухового аналізатора. В кн.:
Оториноларингологія/ Національне керівництво / під ред. В. Т. Пальчуна
В. Т. 2-е видання. – М.: Геотар, 2016. – 1024 с.
- Таварткіладзе Р. А. Керівництво по клінічній аудіології. – М: Медицина, 2013. – 674 с.
- Таварткіладзе
Р. А., Ясінська А. А. Вроджені і перинатальні порушення слуху/ В кн.:
«Неонатологія/ Національне керівництво – короткий видання». – М.:
Геотар, 2013. – Гл.30. – С. 804-816.
- Davis A, Bamford J, Wilson I, Ramkalawan T, Forshaw M, Wright S. A critical review of the role of neonatal hearing screening in the detection of congenital hearing impairment. Health Technol Assess. 1997;1(10):i-iv, 1-176
- Hyde ML. Newborn hearing screening programs: Overview. Journal of Otolaryngology. – 2005. – V. 34, (Suppl 2). – P. 70–78
- Newborn
and infant hearing screening: current issues and guiding principles for
action. Outcome of a WHO informal consultation held at WHO
headquarters, Geneva, Switzerland, 9-10 November, 2009. WHO; 2010.
- American
Academy of Pediatrics, Joint Committee on Infant Hearing Year 2007
position statement: Principles and guidelines for early hearing
detection and intervention programs. Pediatrics. – 2007. – V. 120. –
P. 898–921.
- Дайхес
Н.А., Таварткіладзе Р. А., Яблонський С. В., Ясінська А. А., Гвелесіані
Т. Р., Куян С. М., Загорянская М. Е., Пашков А.с Ст., Гузь Е. В. Універсальний
аудіологічній скринінг новонароджених і дітей першого року
життя//Методична розробка. – М., 2008.
- Гарбарук
Е. С., Королева В. В. Аудіологічній скринінг новонароджених в Росії:
проблеми та перспективи. Посібник для лікарів. Санкт-Петербург, СПб НДІ
вуха, горла, носа й мови. 2013.- 52 с.
- Vos
B, Senterre C, Lagasse R, SurdiScreen Group, Lev?que A. Newborn hearing
screening programme in Belgium: a consensus recommendation on risk
factors. BMC Pediatrics. 2015; 15: 160. doi: 10.1186/s12887-015-0479-4.
- Guidance for Auditory Brainstem Response testing in babies. Version 2.1 NHSP Clinical Group, March 2013. thebsa.org.uk/wp-content/uploads/2014/08/NHSP_ABRn…
- Guidelines
for the early audiological assessment and management of babies referred
from the newborn hearing screening programme. NHSP Clinical Group.
Version 3.1, July 2013.
thebsa.org.uk/wp-content/uploads/2014/08/NHSP_Neon… - Visual Reinforcement Audiometry: Recommended Procedure. British Society of Audiology, June 2014. thebsa.org.uk/wp-content/uploads/2014/06/Visual-Re…
- DeMarcantonio M, Choo DI. Radiographic Evaluation of Children with Hearing Loss. Otolaryngol Clin North Am. 2015;48(6):913-32.
- Clinical practice guideline: sudden hearing loss. Otolaryngol Head Neck Surg. 2012; 146(3) Suppl:1-35.
- Pediatric Amplification Practice Guidelines. American Academy of Audiology, June 2013. audiology.org/sites/default/files/publications/Ped…
Додаткові факти
Приглухуватість – зниження слуху, при якому може мовне спілкування. Глухота – ступінь зниження слуху, при якій хворий не чує слова, вимовлені голосно біля його вуха. Проблема глухоти і приглухуватості набуває великого значення у зв’язку з її широкою поширеністю.
В даний час глухота і клінічно значуща приглухуватість спостерігається у 13 млн. Росіян, причому більше мільйона хворих – діти віком до 18 років. Один новонароджений з тисячі народжується з тотальною глухотою чи глибокої приглухуватістю.
Порушення слуху виявляються у 14% росіян у віці 45-64 роки та у 30% жителів нашої країни у віці старше 65 років. Якщо зниження слуху спостерігається з народження або виникло до того, як дитина починає говорити, така приглухуватість називається ранньою.
Терміни та визначення
Сенсоневральна
приглухуватість (СНП) – форма зниження (аж до втрати слуху, при якій
уражаються які-небудь з ділянок звукосприймаючого відділу слухового
аналізатора, починаючи від безпосереднього сенсорного апарату равлики і
закінчуючи поразкою невральних структур.
Сенсоневральна приглухуватість (СНП) – форма зниження (аж до втрати)
слуху, при якій уражаються які-небудь з дільниць
звукосприймаючого відділу слухового аналізатора, починаючи від
нейроэпителиальных структур внутрішнього вуха і закінчуючи кірковим
представництвом у скроневій частці кори головного мозку, яка виникла у
процесі внутрішньоутробного розвитку плода або в перинатальному періоді.
Класифікація
Відповідно до єдиної міжнародної класифікації (ВООЗ, 1997) в
залежно від тяжкості порушення слуху виділяють наступні ступені
приглухуватості (табл. 1).
Таблиця 1. Міжнародна класифікація ступенів приглухуватості
|
Ступінь приглухуватості |
Середнє значення порогів чутності по повітрю на частотах 500, 1000, 2000, 4000 Гц (дБ) |
|
I |
26-40 |
|
II |
41-55 |
|
III |
56-70 |
|
IV |
71-90 |
|
Глухота |
?91 |
За часом виникнення СНП у дітей може бути вродженою, прогресуючої, пізньою і придбаної.
За принципом гостроти захворювання у дітей виділяють гостру і стійку (хронічну) СНП.
Щодо строків мовленнєвого розвитку СНП у дітей може бути доречевой або послеречевой.
Скринінг
В результаті появи високочутливих об’єктивних методів
дослідження слухового аналізатора, застосовних у новонароджених і не
потребують залучення висококваліфікованого персоналу [18-20]. У
багатьох країнах були реалізовані програми універсального скринінгу
новонароджених [21-23].
Золотим рекомендованим стандартом [24] є:
- Скринінгове дослідження слуху у всіх немовлят у віці до 1 місяця;
- Завершення діагностичного етапу дітям, які не пройшли універсальний аудіологічній скринінг, у віці до 3 місяців;
- Початок індивідуальної програми реабілітації дітям, у яких підтверджено зниження слуху, у віці до 6 місяців.
На сьогоднішній день в якості скринінгового методу для ранньої
діагностики порушень слуху широко застосовується реєстрація затриманої
викликаної амоакустичної емісії (ЗВОАЭ), яка відповідає
критеріями ефективності скринінгу щодо простоти і часу
проведення дослідження та характеризується високою чутливістю навіть
до незначного порушення функціонального стану органа слуху.
Практичне значення ЗВОАЭ полягає в можливості її при реєстрації
умови нормального або близького до норми функціонального стану
рецепторного апарату внутрішнього вуха і збереження звукопровідною
системи.
Як відомо, ЗВОАЭ не реєструється, якщо пороги слуху
перевищують 25-30 дБ нПС в частотному діапазоні від 1 кГц до 4 кГц,
охоплює більшу частину зони мовних частот. Метод є
об’єктивним, простим у виконанні та інтерпретації, характеризується
швидкістю проведення дослідження.
В основі автоматизованої реєстрації ЗВОАЭ лежить дія
запатентованого автоматичного биноминального статистичного тесту –
спеціального математичного алгоритму для проведення точної
статистичної обробки сигналу, заснованої на теорії ймовірності.
Наявність або відсутність ЗВОАЭ автоматизований алгоритм зараховує
як «тест пройдено» – PASS або «тест не пройдено» – REFER, відповідно.
До недоліків методу реєстрації ЗВОАЭ відноситься недостатньо висока
специфічність, що обумовлено завищеним показником
хибнопозитивних результатів (помилково виявлених), складових у
новонароджених у перші добу життя майже 20%.
https://www.youtube.com/watch?v=ytabout
Хибнопозитивні
результати нерідко обумовлені залежністю якості запису ЗВОАЭ від
стану середнього вуха і зовнішнього слухового проходу (негативним
тиском в барабанної порожнини, наявністю післяпологових мас у зовнішньому
слуховому проході і т. п.
), яке розглядається як транзиторне,
фізіологічного стану дітей раннього віку і новонароджених.
Тому оптимальним терміном для проведення реєстрації ЗВОАЭ є
3-4-й день після народження дитини, коли зовнішній слуховий прохід вже
вільний від сторонніх мас і реєстрація емісії найбільш ефективна
Високий рівень помилково не пройшли скринінг c допомогою ЗВОАЭ
невиправдано збільшує час реєстрації і витрати на проведення
дорогих методик при повному аудиологическом обстеженні,
призначуваного на наступному етапі.

Також треба враховувати і моральний аспект
проблеми хибнопозитивних результатів, що полягає у марно
доставленої тривозі годуючій мамі і членам сім’ї помилково виявленого в
плані приглухуватості дитини при наявності у нього нормального слуху, що
негативно впливає на якість життя всієї родини.
До того ж реєстрація
ЗВОАЭ, джерелом якої є зовнішні волоскові клітини равлика, не
забезпечує виявлення ретрокохлеарной патології, що становить майже
10% в структурі високого ступеня приглухуватості і глухоти.
Метод реєстрації коротколатентных слухових викликаних потенціалів
(КСВП) характеризується більш високою чутливістю та специфічністю
у порівнянні з реєстрацією ЗВОАЭ. Однак сам процес запису КСВП
набагато триваліше, більш чутливий до умов проведення
тестування (необхідне забезпечення відповідного стандартам
заземлення), потребує значного технічного забезпечення високої
кваліфікації персоналу.
Технології швидкого автоматизованої реєстрації КСВП дозволяють
значно знизити трудомісткість стандартної запису потенціалів,
забезпечують як високу чутливість і специфічність, так і високу
економічність.
В основі автоматизованої реєстрації КСВП, реалізованої в
скринінгових приладах, лежить дію автоматичного алгоритму
(биноминального статистичного тесту). В приладах використовується
околопороговая інтенсивність стимуляції – 35 дБ нПС, що надається через
внутрішньовушний телефон. При проведенні обстеження передбачається
наклеювання електродів в рекомендованих місцях.
Стаціонарні слухові викликані потенціали (СВП) є версією
КСВП, зареєстровані на високих частотах пред’явлення стимулу. В
внаслідок накладення відповідей при зменшенні інтервалу межстимульного
стволомозговиі потенціали приймають вигляд суворо періодичної функції,
яка трансформується в частотну область і оцінюється за допомогою
спектрального аналізу.
Використовується для визначення стаціонарних СВП
запатентований автоматичний алгоритм – «Fast Steady State Algorithm» –
технічно реалізований в скринінговому обладнанні за слуховим викликаним
потенціалам стовбура мозку, забезпеченим акустичним зондом (суміщення
передпідсилювача, стимулятора, навушника і стаціонарних регульованих
електродів на головному телефоні).
Відповідь визначається в частотній області
при використанні статистичних тестів, що включають в аналіз амплітуду і
фазу основних спектральних частот, відповідних частоті стимулу і
кратних їй високих частотах гармонік стимулу нижче 800 Гц.
Застосовувана
приладі частота стимуляції інтенсивністю 35 дБ нПС дорівнює 90 клацанням в
секунду, при якій у новонароджених середній час детекції відповіді
мінімальне, а частота детекції відповіді — 100%.
Автоматичний алгоритм для визначення стаціонарних СВП, так і
для автоматизованої реєстрації КСВП забезпечує виконання
загальновизнаного для скринінгу правила — простота інтерпретації
отриманих результатів «пройшов — не пройшов тест («PASS» – «REFER»).
Непроходження тесту (результат — «REFER») вказує на можливість порушення слуху (перевищення порогів чутності 35-40 дБ нПС).
Програма універсального аудіологічного скринінгу новонароджених та дітей 1-го року життя
В Росії програма універсального аудіологічного скринінгу
новонароджених та дітей 1-го року життя реалізується з 2008 року на
державному рівні [25]. Протокол програми наказує на 1-му
етапі проведення всім новонародженим реєстрацію ЗВОАЭ на 3-4-ту добу
життя в пологовому будинку, недоношеним дітям реєстрацію ЗВОАЭ проводять в
терміни від 14 днів до 1 місяця.
У разі відсутності чіткої відповіді на одне
або обидва вуха дитині проводять повторну реєстрацію ЗВОАЭ у поліклініці
1 місяць. Також у поліклініці проходять 1-й етап скринінгу діти, у
яких в обмінній карті немає відмітки про проведення аудіологічного
скринінгу, і діти, народжені поза пологового установи.
За
результатами тестування в поліклініці діти з відсутністю чіткої відповіді
на одне або обидва вуха направляються на 2-й етап у центри реабілітації
слуху для проведення розширеного аудіологічного обстеження
віці до 3 місяців.
Міжнародними керівництвами рекомендується використовувати окремий
протокол скринінгу у дітей, що потребують перебування в палатах інтенсивної
терапії понад 48 годин. Цим дітям рекомендовано проведення
автоматичної реєстрації КСВП з метою виключення ймовірності не тільки
сенсоневральної приглухуватості, але і захворювань спектру аудиторних
нейропатій [24, 26].
Значимість факторів ризику вимагає регулярного перегляду по мірі
накопичення та аналізу статистичних даних [27]. В рекомендаціях
Об’єднаного комітету по скринінгу слуху новонароджених у 2007 році [24]
всі патологічні стани неонатального періоду були об’єднані в
одну позицію.
- Рекомендовано направлення на аудіологічне обстеження незалежно
від результатів 1-го етапу скринінгу дітей з наступними факторами ризику
по приглухуватості і глухоті [4-14, 24, 27]:
- Наявність найближчих родичів, які мають порушення слуху з дитинства;
- Синдроми, асоційовані з порушенням слуху;
- Щелепно-лицьові аномалії (за винятком вушних привесков, ізольованою розщілини верхньої губи);
- Внутрішньоутробні інфекції (ЦМВІ, краснуха, токсоплазмоз, сифіліс);
- Перебування у відділенні реанімації та інтенсивної терапії новонароджених більше 48 годин;
- Недоношеність 32 тижні і менше або дуже низька маса тіла (менше 1500 г) при народженні;
- Важка гіпербілірубінемія (більше 200 мкмоль/л у здорових
новонароджених, з поправкою на недоношеність, вимагає замісного
переливання крові);
- Важке гіпоксично-ішемічне/геморагічне ураження центральної нервової системи (ЦНС);
- Застосування ототоксичних препаратів.
Патологія вагітності, якщо вона не позначилася на стані новонародженого, не вважається самостійним чинником ризику. Наявність 2-х і більше факторів ризику підвищує ймовірність розвитку патології слухового аналізатора.
Всі батьки повинні отримувати письмову інформацію про ключових етапах
розвитку слуху, мовлення та мови, а також інформацію про фактори ризику
розвитку прогресуючої приглухуватості або приглухуватості з пізнім початком.
Додаток Ст. Інформація для пацієнтів
На
1-му етапі аудіологічного скринінгу при непроходження тесту батьки
повинні бути поінформовані, що скринінгова процедура є не
діагностикою, а лише відбором на діагностику порушень слуху, яку
необхідно здійснити до 3-х місяців життя.
Тест, заснований на
реєстрації амоакустичної емісії, може бути ложноположителен на тлі
проблем зовнішнього та середнього вуха. Якщо отоакустическая емісія не
зареєстрована при тимпанограмме типу А, то з діагнозом
«сенсоневральна приглухуватість неуточненная» дитина має бути спрямований
на 2-й етап скринінгу в центр реабілітації слуху.
«Перші три роки життя дитина вчиться слухати і говорити. Якщо малюк
погано чує, то він буде погано розуміти мову або зовсім не зможе її
розуміти. З-за цього важко навчитися говорити. Зі зниженим слухом
народжується приблизно 3 малюка з 1000, з них 1 – з глибокими втратами
слуху.
У минулі роки для такої дитини був би закритий світ звуків і
повноцінного життя, у нього б не було мовного спілкування, соціальної
адаптації. Сьогодні з’явились нові можливості ранньої діагностики слуху і
слухоречевого розвитку слабочуючих дітей.
При своєчасній розпочатої
програмою допомоги діти зі зниженим слухом мало чим відрізняються від
однолітків. Вони ходять у звичайні дитячі сади і школи, вчаться грати на
музичних інструментах, вивчають іноземні мови.
Для перевірки слуху використовується швидкий, безболісний і абсолютно
безпечний для здоров’я малюка спосіб. Слух перевіряється на 3-4 день
методом викликаної амоакустичної емісії. Обстеження проводиться у
сні.
При відсутності «луни» ні в якому разі не можна відразу говорити про
приглухуватості. Причинами відсутності «луни» можуть бути: а) наявність
післяпологових мас у зовнішньому слуховому проході; б) захворювання середнього
вуха; в) наявність істинної патології слухової системи.
Якщо «ехо» не зареєстровано, то Вашому малюкові слід повторити обстеження через 1 місяць.
Слух не завжди залишається нормальним і з часом може погіршуватися.
Якщо у вас є сумніви, чи добре дитина чує і розуміє мову, то
негайно зверніться до лікаря і перевірити слух Вашої дитини».
При первинній діагностиці сенсоневральної приглухуватості у дітей
батькам належить ознайомлення з великим об’ємом інформації про
медичній, реабілітаційній, соціальної та освітньої стороні
приглухуватості.
Питання лікування мають особливу актуальність та екстреність при гострій
формі сенсоневральної приглухуватості. Відсутність ефективного лікування
стійкою сенсоневральної приглухуватості з точки зору доказової медицини
вимагає своєчасного початку вибору корекції порушеної слухової
функції.
При односторонній приглухуватості потрібні додаткові диференціально-діагностичні заходи.
За свідченнями пацієнт направляється на медико-соціальну експертизу
(МСЕ) для вирішення питання про надання статусу «дитина-інвалід» з
наступним складанням індивідуальної програми реабілітації та
абилитации (ІПРА) і вибором корекції (традиційне слухопротезування,
імплантанційне слухопротезування, кохлеарна імплантація).
Диференціальна діагностика
Диференціювання між кондуктивної приглухуватістю (ураженням звукопровідного апарату) та нейросенсорної приглухуватістю (патологією апарату звукосприйняття) проводиться за допомогою аудіометрії та отоскопії. У пацієнтів з кондуктивної приглухуватістю при отоскопії можуть виявлятися перфоративні або рубцеві зміни барабанної перетинки.
У ряді випадків (рубці на барабанній порожнині, зрощення стремечка, молоточка і ковадла) зміни при проведенні отоскопического дослідження не виявляються. Рухливість звукопровідною системи оцінюється за допомогою пневматичної воронки Зигле.
Істотну допомогу в процесі диференціальної діагностики між кондуктивної і нейросенсорної приглухуватістю надає порівняльна оцінка повітряної і кісткової провідності. При кондуктивної приглухуватості повітряна звукопровідність погіршується, а кісткова зберігається на нормальному рівні або навіть поліпшується.
Для нейросенсорної приглухуватості характерно погіршення як повітряного, так і кісткової провідності. На аудіограмі пацієнта з кондуктивної приглухуватістю виявляється значний розрив між лініями кісткової та повітряної провідності, на аудіограмі хворого з нейросенсорної приглухуватістю лінії провідності зливаються.
Для визначення локалізації рівня ураження слухового нерва і диференціальної діагностики між нейросенсорної і корковою (що з’явилася в результаті пошкодження відповідних ділянок головного мозку) глухотою необхідна консультація отоневролога.
Застосовуються спеціальні обстеження (порогова аудіометрія, тонова аудіограма, дослідження слухових ВП ). Значні труднощі виникають при виявленні приглухуватості і глухоти у дітей раннього віку.
Профілактика професійної сенсоневральної приглухуватості
- Рекомендовано диспансерне спостереження дитини з підтвердженою
сенсоневральною приглухуватістю у центрі реабілітації слуху [19, 24, 29].
Рівень переконливості рекомендацій – З (рівень достовірності доказів IV)
Протягом усього реабілітаційного процесу батьки, члени сім’ї та
інші обличчя, які допомагають дитині користуватися слуховим апаратом та
кохлеарним імплантом, повинні отримувати постійну професійну
підтримку.
– протягом перших двох років використання слухового апарата – не менш одного разу на три місяці;
– після перших двох років використання слухового апарату – кожні 3-6 місяців;
– після КІ – згідно з клінічними рекомендаціями «Реабілітація пацієнтів після КИ».
Повторні дослідження і спостереження при слухопротезування повинні включати:
-
- Поведінкове аудіологічне дослідження, що включає дослідження по повітряному та кістковому звукопроведению;
- Акустичну импедансометрию для оцінки функції середнього вуха;
- Налаштування параметрів корекції на підставі отриманих даних аудіометрії і вікових змін дитини;
- Електроакустичні виміри слухового апарату;
- Прослуховування слухового апарату;
- Оцінку установки вкладиша;
- Вимірювання з використанням зондувального мікрофона, вимірювання
відмінності між реальним вухом і сполучної камерою і засновані на
цих вимірах зміни налаштувань (з ростом дитини проводиться заміна
індивідуальних вушних вкладишів);
- Вимірювання функціонального посилення з метою відображення розвитку слухових навичок.
При виявленні одностороннього зниження слуху з нормальними порогами в
здоровому вусі необхідно проводити динамічне спостереження за слуховий
функцією, а також розвитком мови і мови кожні 6 міс. до досягнення
дитиною віку 3-х років.
Повторні дослідження і спостереження після кохлеарної імплантації з урахуванням вікових особливостей дитини повинні включати:
- Сурдопедагогическое тестування пацієнта;
- Тональну порогову аудіометрію (ігрову аудіометрію) у вільному полі;
- Реєстрацію потенціалу дії слухового нерва методом телеметрії нервового відповіді;
- Мовну аудіометрію у вільному полі з використанням збалансованих артикуляційних таблиць;
- Налаштування мовного процесора;
- Повторну консультацію сурдопедагога;
- Повторну тональну, мовну аудіометрію у вільному полі.
Основним профілактичним заходом щодо попередження глухоти і приглухуватості є масове обстеження. Регулярні обстеження показані всім працівникам шумних виробництв та іншим категоріям населення, які входять до групи підвищеного ризику.
Дуже важливо своєчасно виявляти ознаки туговухості у дітей, оскільки не виявлені вчасно порушення слуху можуть стати причиною затримки формування мови і відставання в інтелектуальному розвитку.
Міністерство охорони здоров’я Російської Федерації направляє Методичні рекомендації “Діагностика, експертиза працездатності і профілактика професійної сенсоневральної приглухуватості”, підготовлені колективом фахівців ФГБУ ГНЦ “Федеральний Медичний Біофізичний Центр їм.А.І.
Бурназяна”, ФГУП “ФНЦ гігієни ім.Ф.Ф.Ерісмана”, ФГУП “ВНДІ залізничної гігієни” Росспоживнагляду, ФБГУН “Російський науково-практичного центру аудіології та слухопротезування” ФМБА Росії для використання в практичній діяльності.
Т. В. Яковлєва
|
Головний позаштатний спеціаліст профпатолог Міністерства охорони здоров’я Російської Федерації |
||||
|
“ЗАТВЕРДЖУЮ” |
||||
|
“ |
“ |
2012 р. |
||
|
N |
||||
Профілактика ПСНТ повинна бути комплексною, що базується на фізіолого-гігієнічних, організаційних, санітарно-технічних і медичних заходах.Фізіолого-гігієнічне регламентування виробничого шуму передбачає допустимі рівні шуму на робочих місцях.
Шум на робочих місцях нормуються граничними спектрами рівнів звукового тиску (дБ) в октавних смугах частот зі середньогеометричними частотами 31,5; 63; 125; 500; 1000; 2000; 4000 і 8000 Гц і рівнями звуку в дБА у відповідності з СН 2.2.4/2.1.8.

562-96 “Шум на робочих місцях, у приміщеннях житлових, громадських будівель і на території житлової забудови”.”Допустимий” нормований параметр виробничого шуму – рівень шуму, який не викликає ураження органу слуху при щоденному 8-годинному впливі протягом 40-годинного робочого тижня, відповідає еквівалентного рівня шуму 80 дБА (табл.3).
Таблиця 3
|
Нормований |
Октавні смуги з середньогеометричними частотами, Гц |
Еквівалентний |
||||||||
|
параметр. рівні звуку, дБ |
31,5 |
63 |
125 |
250 |
500 |
1000 |
2000 |
4000 |
8000 |
рівень звуку, дБА |
|
Допустимі |
107 |
95 |
87 |
82 |
78 |
75 |
73 |
71 |
69 |
80 |
зменшенням шуму в джерелі його утворення конструктивними, технологічними і експлуатаційними заходами, а також зниженням рівня шуму на шляху його поширення засобами звукоізоляції і звукопоглинання, застосуванням засобів індивідуального захисту (ЗІЗ) органів слуху (протишумні вкладиші, навушники, шоломи (відповідно до ГОСТ Р 12.4.
211-99 “Система стандартів безпеки праці. Засоби індивідуального захисту органу слуху. Протишуми. Суб’єктивний метод вимірювання поглинання шуму”; ГОСТ Р 12.4.208-99 “Система стандартів безпеки праці.
Засоби індивідуального захисту органу слуху. Навушники. Загальні технічні вимоги. Методи випробувань”; ГОСТ Р 12.4.209-99 “Система стандартів безпеки праці. Засоби індивідуального захисту органу слуху. Вкладиші.
Загальні технічні вимоги. Методи випробувань”). Противошумам пред’являється ряд вимог, головними з яких є ефективність ослаблення шуму, зручне і нешкідливе використання.Медичні заходи профілактики ПСНТ полягають у суворому дотриманні регламентів ПМО, визначених чинним наказом Мінздоровсоцрозвитку Росії N 302н від 12 квітня 2011 року, спрямованих на раціональний професійний відбір осіб, які вступають у “шумову” професію (при прийомі на роботу в “шумову” професію), визначення професійної придатності працюючих в умовах впливу виробничого шуму;
https://www.youtube.com/watch?v=ytadvertise
стійкі (3 і більше міс.) зниження слуху (одно-, двостороння сенсоневральна, змішана, кондуктивна приглухуватість будь-якого ступеня вираженості; порушення функції вестибулярного апарата будь-якої етіології.

ПМО при вступі на роботу має важливе значення для подальшого динамічного спостереження за станом слуху, що обумовлює необхідність повноцінного заповнення медичної документації, в тому числі і даних аудіологічного дослідження органа слуху.
Диспансерне спостереження за особами, які працюють в умовах впливу шуму, здійснюється у відповідності з рекомендаціями табл.4. Лікувально-реабілітаційні заходи передбачають усунення факторів ризику розвитку ПСНТ – артеріальної гіпертонії, атеросклерозу, остеохондрозу шийного відділу хребта, патології судин головного мозку, порушень ліпідного обміну;
інтенсифікують обмінні, енергетичні, окисно-відновні процеси клітинного і тканинного метаболізму; поліпшують церебральну гемодинаміку, препарати стимулюючої, седативної терапії і т. п.
1.2 Етіологія та патогенез
Основні причини СНП у дітей можна об’єднати в дві великі групи:
спадкові (генетично детерміновані, сімейні) і
неспадкові (екзогенні). З часу виникнення порушення слуху
можуть бути вродженими (фактор впливає на організм ембріона, плода та
новонародженого) і набутими.
Революційні досягнення молекулярної генетики останніх десятиліть
докорінно змінили розуміння істинної природи вродженої
приглухуватості і визначили перегляд співвідношення (частки) причин
етіологічній структурі.
Зміни генотипу є причиною порушень
слуху у 70% дітей з вродженою та доречевой приглухуватістю, причому в 70-85%
випадків це несиндромальные форми. Більше 100 генів, що кодують мембранні,
регуляторні та структурні білки внутрішнього вуха.
Найбільш часто зустрічаються мутації в гені GJB2. Самої
поширеною в Центральному та Північно-Західному регіонах Росії
є делеція 35delG, в здоровій популяції частота її гетерозиготного
носійства становить 2-6%.
Поширеність даної форми
вродженої приглухуватості в Російській Федерації сьогодні становить більш
50% серед усіх дітей, які мають стійке двостороннє порушення слуху. Ген GJB2
кодує синтез білка коннексина 26, який є структурною
субодиницею коннексиновых каналів, відповідальних за гомеостаз іонів К у
равлику.
Результатом рецесивних мутацій цього гена є
вроджена двостороння несиндромальная сенсоневральна приглухуватість
важкого ступеня і глухота. Раніше такі діти складали групу неясної
етіології, оскільки у більшості з них не обтяжений сімейний анамнез і
відсутні інші фактори ризику по приглухуватості [3].
До синдромів, поєднаним з вродженою СНП, насамперед відносять
синдром Пендреда (ген SLC26A4), синдром Ушера IIA типу (ген USH2A),
бранхио-ото-ренальном синдромі (ген EYA1), синдром Ваарденбурга і
інші.
Найбільш частою причиною вродженої спадкової СНП на сьогоднішній
день вважається вроджена цитомегаловірусна інфекція (ЦМВІ), яка
виявляється у 1% новонароджених у загальній популяції та у 25% недоношених.
В
10% випадків вродженої ЦМВІ розвивається неспецифічна симптоматика, у
половини таких дітей виявляють сенсоневральну приглухуватість. Однак 90%
випадків вродженої ЦМВІ характеризується безсимптомним перебігом, частота
розвитку СНП в цій групі становить 25%.
Інші внутрішньоутробні інфекції в даний час набагато рідше
є причиною вроджених порушень слуху (краснуха – успішна
імунізація, токсоплазмоз [5], сифіліс – своєчасне виявлення і
лікування). Немає переконливих даних про роль герпетичної інфекції у
розвитку вродженої приглухуватості [6]
До патологічних станів перинатального періоду, що надають
негативний вплив на слухову функцію новонародженого, відносять
гіпоксію (оцінка за шкалою Апгар 6 балів за 5 хвилин,
необхідність респіраторної підтримки, ознаки церебральної ішемії)
[7], гіпербілірубінемія [8, 9].
Як правило, ці діти перебувають на
лікуванні у відділенні реанімації та інтенсивної терапії новонароджених [10].
Особливу увагу варто приділяти стану слухової функції у дітей,
народжених раніше строку (гестаційний вік 32 тижні і менше, дуже
низька менше 1500 г маса тіла) [11, 12], у міру розвитку дитини
відбувається дозрівання слухових провідних шляхів.
Однак у зв’язку із загальною
незрілістю недоношеного, множинною супутньою патологією і
тривалим періодом виходжування часто реалізуються патологічні
фактори, перераховані вище [13, 14].
До причин придбаної СНП в дитячому віці ставляться менінгіт,
вірусні дитячі інфекції, застосування ототоксичних препаратів
(аміноглікозиди, діуретики і ін), травми голови (перелом скроневих
кісток/основи черепа), нейродегенеративні захворювання, які
вимагають своєчасного аудіологічного обстеження, лікування і
реабілітації.
Основні медпослуги за стандартами лікування Підібрати лікування штучним інтелектом
Консультації лікарів |
||
Консультація ендокринолога
|
||
Консультація сурдолога
|
||
Нехірургічне лікування |
||
| Транстимпанальное введення ліків | ||
Загальна фармакотерапія
|
||
1.3 Епідеміологія
Вроджена СНП являє собою важливу проблему охорони здоров’я.
Необхідність ранньої діагностики приглухуватості і глухоти обумовлена,
насамперед, прямою залежністю мовного і психічного розвитку
людини, що слабко чує дитини від термінів початку проведення реабілітаційних
заходів.
Рекомендований оптимальний стосовно прогнозу мовного і
психоемоційного розвитку вік постановки остаточного діагнозу і
початку реабілітаційних заходів обмежений 3-6 місяцями життя,
особливо у випадку глибокої втрати слуху.
Тому виявлення СНП у дітей
повинно починатися з періоду новонародженості, що дає можливість
негайно приступити до реабілітаційним заходам. Із збільшенням
віку постановки остаточного діагнозу і початку слухомовний
реабілітації інтеграція дітей з приглухуватістю і глухотою в мовну середу
стає все затруднительней, і ймовірність розвитку грубих порушень
мови, соціальної ізоляції і, отже, інвалідизації у дитини
зростає.
Розрахунки показують, що на кожну 1000 фізіологічних пологів
доводиться народження одного глухого дитини. У 20-40 дітей з 1000
новонароджених з популяції, які потребують інтенсивної терапії, є
глухота або виражені порушення слуху.
Невизначеність і
суперечливість наведених у літературі даних багато в чому залежать від
труднощів, що мають місце при дослідженні слуху у дитини, неточності
ретроспективних оцінок, відсутності стандартів при визначенні різних
форм приглухуватості, флюктуирующей природи деяких форм порушень слуху.
https://www.youtube.com/watch?v=ytpress
Проблеми, що виникають при зіставленні різних масивів
статистичних даних, можуть бути пояснені географічними відмінностями,
епідемічними факторами, а також тим, що в ретроспективний аналіз або
аналіз результатів, отриманих у дітей старшого віку, включаються
випадки прогресуючої приглухуватості або приглухуватості з пізнім початком.
Нарешті, значно ускладнює оцінки і те, що з аналізу практично
виключаються слабкі двосторонні втрати слуху, одностороння
сенсоневральна приглухуватість. З урахуванням усіх зазначених чинників відсоток
дітей, що мають стійкі порушення слуху, збільшується до 3-4 на 1000
[15-17].
Епідеміологічні дослідження свідчать про переважно
сенсоневральном типі вроджених порушень слуху (близько 80% у структурі
вродженої приглухуватості). Випадки вродженої СНП історично виявлялись
тільки з причини затримки мовленнєвого розвитку на відміну від порушень
кондуктивного характеру, найчастіше обумовлених вадами розвитку вуха і
іншими щелепно-лицьовими аномаліями.
Клініки для лікування з найкращими цінами
|
| Підібрані клініки | Телефони | Місто (метро) | Рейтинг | Ціна послуг |
| НИАРМЕДИК на Сретенці | 7(495) 617..показатиЗапис: 7(499) 116-82-39
7(495) 617-11-71 |
Москва (м. Стрітенський Бульвар) | 14780ք(80%*) |
2.1 Скарги і анамнез
Основними скаргами при СНП у дітей є відсутність або
сумнівна реакція на звуки у дітей в доречевом періоді на думку
батьків або лікарів-фахівців, затримка мовленнєвого розвитку у дітей
молодшого віку, зниження слуху у дітей старшого віку.
Серед даних анамнезу особливу увагу варто приділяти стану
слуху у найближчих родичів, перебігу вагітності, гестационному
віком на момент пологів, особливостей перебігу пологів, при масі тіла
народження, оцінки за шкалою Апгар, перебігу перинатального періоду, наявності
інфекційних і соматичних захворювань, диспансерному спостереженню у
інших фахівців.
Додаток А1. Склад робочої групи
• Антигіпоксантів і антиоксиданти.
Фармакологічна дія – антигіпоксичну, що регулює енергетичний метаболізм. Фармакодинаміка. Механізм дії. Триметазидин запобігає зниження внутрішньоклітинної концентрації АТФ шляхом збереження енергетичного метаболізму клітин у стані гіпоксії.
Таким чином триметазидин забезпечує нормальне функціонування мембранних іонних каналів, трансмембранний перенос іонів калію і натрію та збереження клітинного гомеостазу. Триметазидин інгібує окислення жирних кислот за рахунок селективного інгібування ферменту 3-кетоацил-КоА-тіолази — мітохондріальної длинноцепочечной ізоформи жирних кислот, що призводить до посилення окислення глюкози та прискоренню гліколізу з окисленням глюкози, що і обумовлює захист міокарда від ішемії.
Переключення енергетичного обміну з окислення жирних кислот на окислення глюкози лежить в основі фармакологічних властивостей триметазидину. Фармакодинамічні властивості. Триметазидин підтримує енергетичний метаболізм серця та нейросенсорных тканин під час ішемії;
зменшує вираженість внутрішньоклітинного ацидозу і змін трансмембранного іонного потоку, що виникають при ішемії; знижує рівень міграції та інфільтрації полинуклеарных нейтрофілів в ішемізованих і реперфузированных тканинах серця;
зменшує розмір пошкодження міокарда; не надає пряме вплив на показники гемодинаміки. У пацієнтів зі стенокардією триметазидин збільшує коронарний резерв, тим самим сповільнюючи наступ ішемії, спричиненої фізичним навантаженням, починаючи з 15-го дня терапії;
обмежує коливання артеріального тиску, викликані фізичним навантаженням, без значних змін ЧСС; значно знижує частоту приступів стенокардії і потреби в прийомі нітрогліцерину короткої дії; покращує скоротливу функцію лівого шлуночка у пацієнтів з ішемічною дисфункцією.
Результати проведених клінічних досліджень підтвердили ефективність і безпека застосування триметазидину у пацієнтів зі стабільною стенокардією, як у монотерапії, так і у складі комбінованої терапії при недостатньому ефекті інших антиангінальних ЛЗ.
У дослідженні з участю 426 пацієнтів зі стабільною стенокардією додавання триметазидину (60 мг/добу) до терапії метопрололом у дозі 100 мг/добу (50 мг 2 рази на добу) протягом 12 тижнів статистично достовірно покращило результати навантажувальних тестів та клінічні симптоми порівняно з плацебо.
Загальна тривалість навантажувальних тестів склала 20,1 с (р=0,023), загальний час виконання навантаження 0,54 METs (р=0,001), час до розвитку депресії сегмента ST на 1 мм 33,4 с (р=0,003), час до розвитку нападу стенокардії 33,9 з (р.
У дослідженні з участю 223 пацієнтів зі стабільною стенокардією додавання триметазидину в дозі 35 мг (2 рази на добу) до терапії атенололом у дозі 50 мг (1 раз на добу) протягом 8 тижнів через 12 год після прийому призводило до збільшення часу до розвитку ішемічної депресії сегмента ST на 1 мм ( 34,4 с, р=0,03) при проведенні навантажувальних тестів у підгрупі пацієнтів (N=173) порівняно з групою плацебо.
Аналогічні результати отримано і для часу розвитку нападів стенокардії (р=0,049). Не виявлено достовірні відмінності між групами для інших вторинних кінцевих точок (загальна тривалість навантажувальних тестів, загальний час навантаження і клінічні кінцеві точки).
У дослідженні з участю 1962 пацієнтів зі стабільною стенокардію триметазидин в двох дозах (70 і 140 мг/добу) у порівнянні з плацебо був доданий до терапії атенололом 50 мг/добу. В загальній популяції, включаючи пацієнтів без симптомів, так і з симптомами стенокардії, триметазидин не продемонстрував переваг ергометричними (загальна тривалість навантажувальних тестів, час до настання ішемічної депресії сегмента ST на 1 мм і час до розвитку нападу стенокардії) і клінічним кінцевим точкам.
Однак у ретроспективному аналізі в підгрупі пацієнтів з симптомами стенокардії (N=1574) триметазидин (140 мг) значно поліпшив загальний час навантажувального тесту ( 23,8 с у порівнянні з 13,1 з плацебо;
Абсорбція. Пролонговане вивільнення. Після прийому всередину триметазидин має лінійний фармакокінетичний профіль і досягає Cmax в плазмі приблизно через 14 год після прийому. В інтервалах між прийомами ( тд;
протягом 24 год) концентрація триметазидину у плазмі крові протягом 15 год після прийому зберігається на рівні не менше 75% від Cmax. Рівноважний стан досягається після прийому 3-ї дози (через 3 доби).
Прийом їжі не впливає на біодоступність триметазидину. Модифіковане вивільнення. Після прийому всередину триметазидин швидко абсорбується, Tmax в плазмі крові становить приблизно 5. Понад 24 год концентрація триметазидину у плазмі крові залишається на рівні, що перевищує 75% концентрації, яка визначається через 11 Рівноважний стан достигаетчся через 60 Прийом їжі не впливає на біодоступність триметазидину.
Розподіл. Vd складає 4,8 л/кг, що свідчить про хорошому розподілі триметазидину в тканинах (ступінь зв’язування з білками плазми крові достатньо низька, приблизно 16% in vitro). Виведення.
Триметазидин виводиться в основному нирками, головним чином у незміненому вигляді. T1/2 у молодих здорових добровольців близько 7 год, у пацієнтів старше 65 років — близько 12. Нирковий кліренс триметазидину прямо корелює з кліренсом креатиніну, печінковий кліренс знижується з віком пацієнта.
Особливі групи пацієнтів. Пацієнти старше 75 років. У пацієнтів старше 75 років може спостерігатися підвищена експозиція триметазидину з-за вікового зниження функції нирок. Було проведено спеціальне дослідження в популяції пацієнтів старше 75 років при прийомі триметазидину в дозі 35 мг 2 рази на добу.
Аналіз, проведений кінетичним популяционным методом, показав в середньому дворазове підвищення експозиції триметазидину у плазмі крові у пацієнтів з тяжким ступенем ниркової недостатності (Cl креатиніну Cl креатиніну 60 мл/хв.
Ніяких особливостей, що відносяться до безпеки триметазидину у пацієнтів старше 75 років порівняно з загальною популяцією, виявлено не було. Ниркова недостатність. Експозиція триметазидину в середньому була збільшена в 2,4 рази у пацієнтів з нирковою недостатністю помірного ступеня тяжкості (Cl креатиніну 30-60 мл/хв) і в середньому в 4 рази — у пацієнтів з тяжким ступенем ниркової недостатності (Cl креатиніну.
Ніяких особливостей, що відносяться до безпеки триметазидину у цій популяції пацієнтів у порівнянні з загальною популяцією, виявлено не було. Діти і підлітки. Фармакокінетика триметазидину у дітей та підлітків віком до 18 років не вивчалася.
Бобошко Марія Юрьевна3, д. м. н., член медичної асоціації, конфлікт інтересів відсутній.
Гарбарук Катерина Сергеевна3, к. б.н., член медичної асоціації, конфлікт інтересів відсутній.
Маркова Тетяна Геннадьевна1,2, д. м. н., член медичної асоціації, конфлікт інтересів відсутній.
Таварткіладзе Георгій Абелович1,2, д. м. н., професор, член медичної асоціації, конфлікт інтересів відсутній.
Циганкова Євгена Ростиславовна1,2, к. м. н., доцент, член медичної асоціації, конфлікт інтересів відсутній.
Чибісова Світлана Станиславовна1,2, член медичної асоціації, конфлікт інтересів відсутній.
https://www.youtube.com/watch?v=upload
Установи-розробники:
- ФГБУН Російський науково-практичного центру аудіології та слухопротезування ФМБА Росії.
- ФГБОУ ДПО РМАНПО Моз україни, кафедра сурдології.
- Лабораторія слуху та мови НДЦ Першого Санкт-Петербурзького
державного медичного університету імені академіка В. П. Павлова.


